多発性骨髄腫はリンパ球の中でBリンパ球の最終分化型である形質細胞の腫瘍性増
殖(骨髄腫細胞)と骨髄腫細胞が産生する単クローン性免疫グロブリン(M蛋白)および
骨髄腫細胞と骨髄の間質細胞の細胞間相互作用によって産生されるサイトカインなどの
液性因子によって多彩な臨床症状を呈する疾患です。
殖(骨髄腫細胞)と骨髄腫細胞が産生する単クローン性免疫グロブリン(M蛋白)および
骨髄腫細胞と骨髄の間質細胞の細胞間相互作用によって産生されるサイトカインなどの
液性因子によって多彩な臨床症状を呈する疾患です。
疫学
人口10万人あたりの推計罹病率は男性においては2.2、女性においては1.7と報告さ
れ、欧米白人に比較すると半分以下となります。年齢では加齢に伴い(特に50歳以降)
罹病率は高くなります(日本骨髄腫研究会は初診時年齢中央値男性65歳、女性67歳、
全体では66歳と報告しております)。
れ、欧米白人に比較すると半分以下となります。年齢では加齢に伴い(特に50歳以降)
罹病率は高くなります(日本骨髄腫研究会は初診時年齢中央値男性65歳、女性67歳、
全体では66歳と報告しております)。
臨床症状
初診時主訴で最も多く見られるのが骨痛であり、貧血に伴う動悸、息切れ、全身倦怠
感によるものが続きます。逆に自覚症状がなく健診で貧血(血算では時に白血球減少、
血小板減少を伴うことがあります)、血清蛋白増加、蛋白尿(ベンスジョーンズ蛋白)など
の検査値異常を指摘されて血液内科に紹介される症例も存在します。
感によるものが続きます。逆に自覚症状がなく健診で貧血(血算では時に白血球減少、
血小板減少を伴うことがあります)、血清蛋白増加、蛋白尿(ベンスジョーンズ蛋白)など
の検査値異常を指摘されて血液内科に紹介される症例も存在します。
他の症状としては骨吸収の亢進による高カルシウム血症(症状としては口渇、多飲、多
尿、便秘、悪心嘔吐、意識障害)が認められます。
尿、便秘、悪心嘔吐、意識障害)が認められます。
(1)骨病変
骨病変は溶骨病変が主であり、この骨病変の評価に最も多く使用されているのが単純
X線検査です。その特徴的な所見が打ち抜き像(punched-out lesion)であり、これは骨
髄腫細胞が骨芽細胞の作用を抑制し、骨融解をきたした病変部位において骨形成を生
じさせないことが原因です。骨痛を生じている症例においては脊椎骨では圧迫骨折や骨
粗鬆症、長管骨においても病的骨折を認めることがあります。単純X線検査は有用な検
査ですが、これによって打ち抜き像あるいは骨折が認められるということは進行性病変
であることを示しており、初期病変の感度は低くなります。全身骨X線所見は4段階で評
価され、0:正常、1:骨粗鬆症、2:骨融解病、3:多発性骨融解病変に分類されていま
す。骨病変評価において問題となるのは高齢者における骨粗鬆症と骨髄腫の骨病変と
の鑑別となります。また単純X検査では治療後の骨病変の評価が困難であり、最近では
CT(マルチスライスCTにより全身撮影が1度で可能)あるいはMRI(全身骨評価は1度で
は困難)による評価が同時に施行されております。
X線検査です。その特徴的な所見が打ち抜き像(punched-out lesion)であり、これは骨
髄腫細胞が骨芽細胞の作用を抑制し、骨融解をきたした病変部位において骨形成を生
じさせないことが原因です。骨痛を生じている症例においては脊椎骨では圧迫骨折や骨
粗鬆症、長管骨においても病的骨折を認めることがあります。単純X線検査は有用な検
査ですが、これによって打ち抜き像あるいは骨折が認められるということは進行性病変
であることを示しており、初期病変の感度は低くなります。全身骨X線所見は4段階で評
価され、0:正常、1:骨粗鬆症、2:骨融解病、3:多発性骨融解病変に分類されていま
す。骨病変評価において問題となるのは高齢者における骨粗鬆症と骨髄腫の骨病変と
の鑑別となります。また単純X検査では治療後の骨病変の評価が困難であり、最近では
CT(マルチスライスCTにより全身撮影が1度で可能)あるいはMRI(全身骨評価は1度で
は困難)による評価が同時に施行されております。
(2)腎障害
多発性骨髄腫症例の約25%に診断時血清クレアチニン上昇が認められます。腎障害
の要因としては脱水、高カルシウム血症、造影剤投与、骨痛などで使用される非ステロ
イド抗炎症薬、降圧剤であるACE阻害薬などがあります。また前述したベンスジョーンズ
蛋白を含め、免疫グロブリンを構成している軽鎖(κ鎖orλ鎖))が糸球体で濾過、近位
尿細管で再吸収され(この際、近位尿細管を障害)、過剰分は遠位尿細管に運ばれてこ
こで円柱構造物を形成、これによって尿細管閉塞が起こり、腎障害が発症します。
の要因としては脱水、高カルシウム血症、造影剤投与、骨痛などで使用される非ステロ
イド抗炎症薬、降圧剤であるACE阻害薬などがあります。また前述したベンスジョーンズ
蛋白を含め、免疫グロブリンを構成している軽鎖(κ鎖orλ鎖))が糸球体で濾過、近位
尿細管で再吸収され(この際、近位尿細管を障害)、過剰分は遠位尿細管に運ばれてこ
こで円柱構造物を形成、これによって尿細管閉塞が起こり、腎障害が発症します。
臨床検査
(1)M蛋白の確認
血清蛋白分画でM蛋白検出を行います。γグロブリン分画にM蛋白が見られますが、
IgAがM蛋白の場合にはβ分画にピークがくることがあるので注意を要します。またベン
スジョーンズ型、IgD型ではピークが認められず、逆に正常免疫グロブリン低下に伴いγ
グロブリン分画の平低化がみられます。
IgAがM蛋白の場合にはβ分画にピークがくることがあるので注意を要します。またベン
スジョーンズ型、IgD型ではピークが認められず、逆に正常免疫グロブリン低下に伴いγ
グロブリン分画の平低化がみられます。
M蛋白が確認されれば血清免疫電気泳動法でM蛋白を確認します。微量なM蛋白の確
認は免疫固定法によって行われます。
認は免疫固定法によって行われます。
(2)骨髄腫細胞の確認
骨髄穿刺、生検により骨髄腫細胞の増殖を確認します。骨髄中の形質細胞比率、形
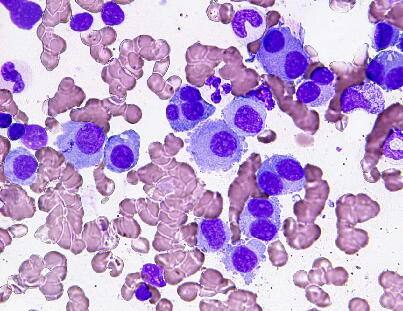
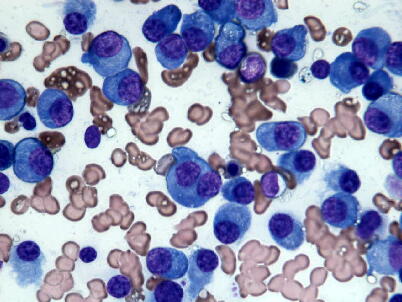
態異常(下図:2核、3核の骨髄腫細胞)により多発性骨髄腫の診断は可能ですが、補助
診断として細胞表面形質分析が有用となることがあります。
態異常(下図:2核、3核の骨髄腫細胞)により多発性骨髄腫の診断は可能ですが、補助
診断として細胞表面形質分析が有用となることがあります。
(a) 染色体検査
従来、染色体分析は核分裂像が得られることが必要なのですが骨髄腫細胞は分裂像
が得にくいために骨髄腫の染色体検索を困難としておりました。現在ではfluorescence
in situ hybridization(FISH)法の導入によって骨髄腫の染色体解析が行われておりま
す。
が得にくいために骨髄腫の染色体検索を困難としておりました。現在ではfluorescence
in situ hybridization(FISH)法の導入によって骨髄腫の染色体解析が行われておりま
す。
代表的な染色体異常としてt(11;14)、t(4;14)、t(8;14)、del(13)、del(17)があります。他
の造血器悪性腫瘍と同様に染色体検査と予後は密接に関係しており多発性骨髄腫の
場合にはt(4;14)、del(13)、del(17)は予後不良とされています(Ref 1, Ref 2, Ref 3)。
del(13)は未治療多発性骨髄腫患者の約50%に認められ、MGUSにも認められます。
MGUSの場合には骨髄腫への進展をきたしやすいこと、多発性骨髄腫の場合には多剤
併用化学療法、移植療法に対しても抵抗性であり、予後不良と報告されております。逆
にt(11;14)例は大量化学療法施行例で予後良好と報告されています。
の造血器悪性腫瘍と同様に染色体検査と予後は密接に関係しており多発性骨髄腫の
場合にはt(4;14)、del(13)、del(17)は予後不良とされています(Ref 1, Ref 2, Ref 3)。
del(13)は未治療多発性骨髄腫患者の約50%に認められ、MGUSにも認められます。
MGUSの場合には骨髄腫への進展をきたしやすいこと、多発性骨髄腫の場合には多剤
併用化学療法、移植療法に対しても抵抗性であり、予後不良と報告されております。逆
にt(11;14)例は大量化学療法施行例で予後良好と報告されています。
(b)細胞表面形質分析
| 正常形質細胞 | CD19陽性・CD20陰性・CD56陰性 |
| 骨髄腫細胞 | ・CD19陰性・CD20陰性 そのうち55-65%がCD56陽性、25-35%がCD56陰性 ・CD19陰性・CD20陽性になるものが15-20% ・CD19陽性・CD56陽性となるものが1-3% |
| monoclonal gammapathy of undetermined significance (MGUS) |
CD19陰性・CD56陽性、CD19陰性・CD56陰性 正常系列と考えられるCD19陽性・CD56陰性が混在 |
CD19、CD20、CD56で分類された骨髄腫細胞は更にMPC-1、CD49e、CD45抗原の
有無によって以下のように分類されます。未熟型は進行型骨髄腫に多い事が報告され
ています。
有無によって以下のように分類されます。未熟型は進行型骨髄腫に多い事が報告され
ています。
| |
MPC-1陰性・CD49e陰性・CD45陽性細胞あるいはMPC-1陰性・CD49e陰性・CD45陰性細胞 |
| |
MPC-1陽性・CD49e陰性・CD45陰性細胞あるいはMPC-1陽性・CD49e陰性・CD45陽性細胞 |
| |
MPC-1陽性・CD49e陽性・CD45陽性細胞 |
(3)血液生化学検査
M蛋白の存在により血清総蛋白値の高値が認められますが、ベンスジョーンズ型、IgD
型、非分泌型では正常免疫グロブリンが抑制されるため、逆に総蛋白値が低下する場
合があり、注意を要します。その他にアルブミン値が低下、BUN、クレアチニン、ALP、
LDH、尿酸、カルシウム、CRP値、βミクログロブリン値が上昇します。βミクログロブリ
ン値は腎障害の指標にもなりますが骨髄腫細胞活動性のマーカーとしても有用であり、
新しい国際病期分類ではアルブミン値とβミクログロブリン値が取り入れられています。
型、非分泌型では正常免疫グロブリンが抑制されるため、逆に総蛋白値が低下する場
合があり、注意を要します。その他にアルブミン値が低下、BUN、クレアチニン、ALP、
LDH、尿酸、カルシウム、CRP値、βミクログロブリン値が上昇します。βミクログロブリ
ン値は腎障害の指標にもなりますが骨髄腫細胞活動性のマーカーとしても有用であり、
新しい国際病期分類ではアルブミン値とβミクログロブリン値が取り入れられています。
診断基準
多発性骨髄腫はmonoclonalなM蛋白を産生し、骨破壊をもたらす形質細胞腫瘍です。
これまでにも種々の診断基準が用いられてきました。2003年にInternational Myeloma
Working Groupが多発性骨髄腫および関連疾患の診断基準を報告しました。これまで
の分類、多く使用されてきたSouthwest Oncology Group(SWOG)分類(下記)とは異な
り、骨髄中の形質細胞比率やM蛋白量に偏った評価はせずに臓器障害の存在を重視し
た基準になっております。
これまでにも種々の診断基準が用いられてきました。2003年にInternational Myeloma
Working Groupが多発性骨髄腫および関連疾患の診断基準を報告しました。これまで
の分類、多く使用されてきたSouthwest Oncology Group(SWOG)分類(下記)とは異な
り、骨髄中の形質細胞比率やM蛋白量に偏った評価はせずに臓器障害の存在を重視し
た基準になっております。
International Myeloma Working Group診断基準(Ref 6)
| monoclonal gammapathy of undetermined significance (MGUS) ・血清M蛋白<3g/dl
・骨髄におけるクローナルな形質細胞比率<10%
・他のB細胞増殖性疾患が否定されること
・臓器障害がないこと
*以前は良性単クローン性高γグロブリン血症と呼ばれていましたが、骨髄腫への移行が認められためMGUSと称されております。多発性骨髄腫への進展率は年間およそ1%、累積進展率は10年で12%と報告されています。
|
| 無症候性骨髄腫 ・血清M蛋白<3g/dl
and/or
・骨髄におけるクローナルな形質細胞の比率≧10%
・臓器障害がないこと
*以前はくすぶり型骨髄腫と呼ばれていました。骨髄腫の診断基準を満たすものの臓器障害がないものを指しております。症候性骨髄腫への移行が認められるため(約2年)、慎重な経過観察を必要とします。
|
| 症候性骨髄腫 ・血清and/or尿にM蛋白を検出
・骨髄におけるクローナルな形質細胞の増加あるいは形質細胞腫
・臓器障害の存在
|
| 非分泌型骨髄腫 ・血清および尿にM蛋白を検出しない(免疫固相法による確認)
・骨髄におけるクローナルな形質細胞の比率≧10%増加または形質細胞腫
・臓器障害の存在
*M蛋白を産生しているが分泌しない症例を指します(1%程度)。骨髄生検などを材料とした酵素抗体法で骨髄腫細胞内に免疫グロブリンを同定します。確定診断には血清中にM蛋白がないことを証明する必要があり、感度のよい免疫固定法での検索が必要です。
|
| 孤発性骨形質細胞腫 ・血清and/or尿にM蛋白を検出しない(時に少量のM蛋白を検出することがある)
・クローナルな形質細胞の増加によるただ1カ所の骨破壊
・正常骨髄
・病変部以外は正常な全身骨所見(X-PおよびMRI)
・臓器障害がないこと
*全形質細胞腫瘍の5%を占め、主たる病変部位は脊椎(骨痛、病的骨折で発症)、発症年齢中央値は55歳で男性に多いと報告されております。予後は放射線療法のみでも比較的良好ですが、進行すると症候性骨髄腫への移行が認められます。
|
髄外性形質細胞腫
・血清and/or尿にM蛋白を検出しない(時に少量のM蛋白を検出することがある)
・クローナルな形質細胞による髄外腫瘤
・正常骨髄
・正常な全身骨所見
・臓器障害がないこと
*骨、骨髄以外の臓器・組織の形質細胞腫は全形質細胞腫瘍の3-5%を占めます。咽喉頭、副鼻腔が主たる病変部位となります。
|
多発性形質細胞腫
・血清and/or尿にM蛋白を検出しない(時に少量のM蛋白を検出することがある)
・1ヶ所以上のクローナルな形質細胞による骨破壊または髄外腫瘤
・正常骨髄
・正常な全身骨所見
・臓器障害がないこと
*形質細胞腫のうち多発する症例が5%認められます。多発性であるため放射線療法のみでは病勢コントロールは困難であり、化学療法、自家移植が必要となります。
|
形質細胞白血病
・末梢血形質細胞>2,000/μl
・白血球分画中形質細胞比率≧20%
*初発骨髄腫患者の2〜4%が形質細胞白血病の病像を呈します。初診時より白血病の病像を示す原発性形質細胞白血病と骨髄腫の経過中に白血化する二次性形質細胞白血病とに分類されます。原発性形質細胞白血病の発症年齢中央値は50-55歳で症候性骨髄腫と比較すると10歳程度若く、男性にやや多く認められます。骨病変は少なく、髄外病変が多く見られます
|
臓器障害
1.高カルシウム血症:血清カルシウム>11mg/dlまたは基準値より1mg/dlを超える上昇
2.腎不全:血清クレアチニン>2mg/dl
3.貧血:Hb値が基準値より2g/dl以上低下または10g/dl未満
4.骨病変:溶骨病変または圧迫骨折を伴う骨粗鬆症(MRIあるいはCT)
5.その他:過粘稠症候群、アミロイドーシス、年2回以上の細菌感染
|
病期分類
従来、病期分類は1975年に発表されたDurie&Salmonの分類(Ref 7)が使用されてき
ました。病期II、IIIが治療対象とされ、臨床上、重要な分類となっておりましたが、近年、
予後因子の解明が進み、見直されてきております。単変量解析ではPerformance
status(PS)、年齢、腎機能、血清β2‐ミクログロブリン、血清アルブミン、LDH、CRP、
labeling index(腫瘍増殖能)、骨髄腫細胞形態などが報告されています。この中ではβ
2‐ミクログロブリン(β2M)とアルブミン値を予後因子として組み合わせた病期分類が発
表あされており、迅速な結果が得られるこの2つの因子を組み合わせた病期分類は治
療戦略に重要な役割を果たすものと考えられます。
ました。病期II、IIIが治療対象とされ、臨床上、重要な分類となっておりましたが、近年、
予後因子の解明が進み、見直されてきております。単変量解析ではPerformance
status(PS)、年齢、腎機能、血清β2‐ミクログロブリン、血清アルブミン、LDH、CRP、
labeling index(腫瘍増殖能)、骨髄腫細胞形態などが報告されています。この中ではβ
2‐ミクログロブリン(β2M)とアルブミン値を予後因子として組み合わせた病期分類が発
表あされており、迅速な結果が得られるこの2つの因子を組み合わせた病期分類は治
療戦略に重要な役割を果たすものと考えられます。
SWOG病期分類(Ref 8)
| |
|
|
| Stage 1 | |
|
| Stage 2 | |
|
| Stage 3 | |
|
| Stage 4 | |
|
International Staging System(Ref 9)
| |
|
|
| Stage 1 | |
|
| Stage 2 | |
|
| Stage 3 | |
|
(補)
SWOGの骨髄腫および関連疾患の診断基準
| 1.multiple myeloma | major criteria (I) 生検で形質細胞腫の確認 (II)骨髄で形質細胞が30%以上 (III)M蛋白の存在 IgG>3.5g/dl IgA>2.0g/dl BJP>1.0g/日(アミロイドーシスなし) |
| minor criteria (a)形質細胞比率10〜30% (b)M蛋白は存在するが、上記以下である (c)骨融解像が認められる (d)正常免疫グロブリンの低下 IgG<600mg/dl、IgA<100mg/dl、IgM<50mg/dl |
|
| 進行性で症状を有する症例で、以下の場合多発性骨髄腫とする 1:I+b, I+c, I+d 2:II+b, II+c, II+d 3:III+a, III+c, III+d 4:a+b+c, a+b+d |
|
| 2.MGUS | (I)M蛋白の存在 (II)M蛋白の量が以下の基準を満たす IgG≦3.5g/dl IgA≦2.0g/dl BJP≦1.0g/日 (III)骨髄で形質細胞が10%未満 (IV)骨病変を認めない (V)症状がない |
| 3.非活動性骨髄腫 | 骨髄腫の診断基準を満たし、かつ下記の基準を満たす (I)3ヶ所以下の溶骨病変(圧迫骨折を認めない) (II)M蛋白の量が以下を満たす IgG<7g/dl IgA<5g/dl (III)症状がなく、以下を満たす performance status(Karnofsky scale)>70% ヘモグロビン値>10g/dl 血清カルシウム値が正常 血清クレアチニン値<2.0mg/dl 感染症を認めない |
| 4.くすぶり型骨髄腫 | 非活動性骨髄腫の診断基準を満たし、かつ以下の基準を満たす (I)骨病変を認めない (II)骨髄で形質細胞が10〜30% |
Durie & Salmonの病期分類
| |
基準 |
| |
次の項目をすべて満たすもの 1.ヘモグロビン値>10g/dl 2.血清カルシウム値正常 3.骨レントゲン写真(正常像あるいは孤立性骨病変) 4.M蛋白成分低値 IgG<5g/dl IgA<3g/dl 尿中BJP<4g/日 |
| |
病期I、IIIIのいずれにも属さないもの |
| |
次の項目のうち1つ以上を認めるもの 1.ヘモグロビン値<8.5g/dl 2.血清カルシウム値>12mg/dl 3.進行した骨病変(広範囲および骨折) 4.M蛋白成分高値 IgG>7g/dl IgA>5g/dl 尿中BJP>12g/日 |
平成20年4月1日初稿
|
|

